学院研究团队破译“鱼和熊掌”兼得密码 研发兼具高压电性与高柔性的超柔性有机压电薄膜
兰州大学材料与能源学院刘书海青年教授研究团队在有机压电材料领域取得重要突破,他们提出液-液界面极性工程策略成功攻克有机压电材料领域长期存在的高压电性与高柔性难以协同的共性难题。相关成果以“Ultra-soft organic combined film with piezoelectricity induced by liquid-liquid interface polar engineering”为题于2025年7月11日发表在国际权威期刊《Nature Communications》(DOI: 10.1038/s41467-025-61526-2),为研制下一代可植入式生物医疗传感器和自适应可穿戴设备奠定了关键材料支撑。

有机压电材料(如PVDF、聚乳酸等)因其固有的生物相容性,成为制造生物力学传感器(用于检测生物组织/器官的收缩、扩张、挤压和蠕动等运动信号)的理想选择。然而,此类材料长期面临两大瓶颈:压电性远低于无机材料;且柔量(杨氏模量的倒数)较人体组织相比低3到6个数量级。这一性能受限的关键在于两个方面。其一,高极性分子的规则、致密排列和高结晶度是获得强压电响应的关键。这通常会使分子链间存在较强的(如偶极-偶极、氢键)相互作用(形成较高的空间位阻),以利于实现稳定的极性排列(极化)。然而,强相互作用和高结晶度会严重限制分子链的内旋和滑移,导致材料变硬。其二,高柔性则需要材料具有类似橡胶态的特性,其分子链高度无规缠绕,链段具有极大的运动自由度(低空间位阻效应),分子链间作用力较弱(如范德华力)。这种高度无序、松弛的结构允许材料在微小应力下发生大变形。然而,这种高度无序的结构恰恰阻碍了分子链或极性基团的规则取向和稳定极化。即使在强外电场下诱导出部分极化,这种无序结构也难以将极化状态有效“冻结”(保持),导致压电性难以提高甚至下降。在传统的有机压电材料(如PVDF)或其复合材料体系中,追求高结晶度或强分子间相互作用以增强压电性,不可避免地会牺牲分子链的运动性,导致材料变硬(柔性降低);反之,为了获得接近生物组织的超高柔性而引入柔性链段、增塑剂或设计低密度交联网络,则会显著破坏分子的规则排列和极化效率,从而削弱压电性。因此,传统的分子自组装或复合策略虽能单一提升压电性或柔性,但始终无法破解“提压电则损柔性,增柔性则弱压电”的困境,难以满足生物力学传感器对高柔软度和高灵敏度的“双高”需求,大大限制了其实际应用。
针对这一问题,研究团队提出了一种液-液界面极性工程策略(liquid-liquid interface polar engineering,图1),利用线性聚合物(低位阻效应)聚乙二醇(PEG)与聚苯乙烯-嵌段-聚异戊二烯-嵌段-聚苯乙烯共聚物(SIS)在甲苯-水界面的极性差异,驱动相分离形成稳定极性不对称结构,进而在低模量复合材料体系中产生压电性。实验结果显示,基于该策略构建的PEG/SIS薄膜不仅展现出高达22.9 pC/N的压电系数,性能稳定,在60天内无衰减,与天然有机材料PVDF的压电性相当,还具有与皮肤、软骨和主动脉相似的超高柔软度(1/E约为1×10–6 Pa–1),显示出与生物组织的高度机械顺应性。这项工作为设计新型高性能有机压电材料提供了新的思路,有望推动其在生物力学传感器领域的实际应用。
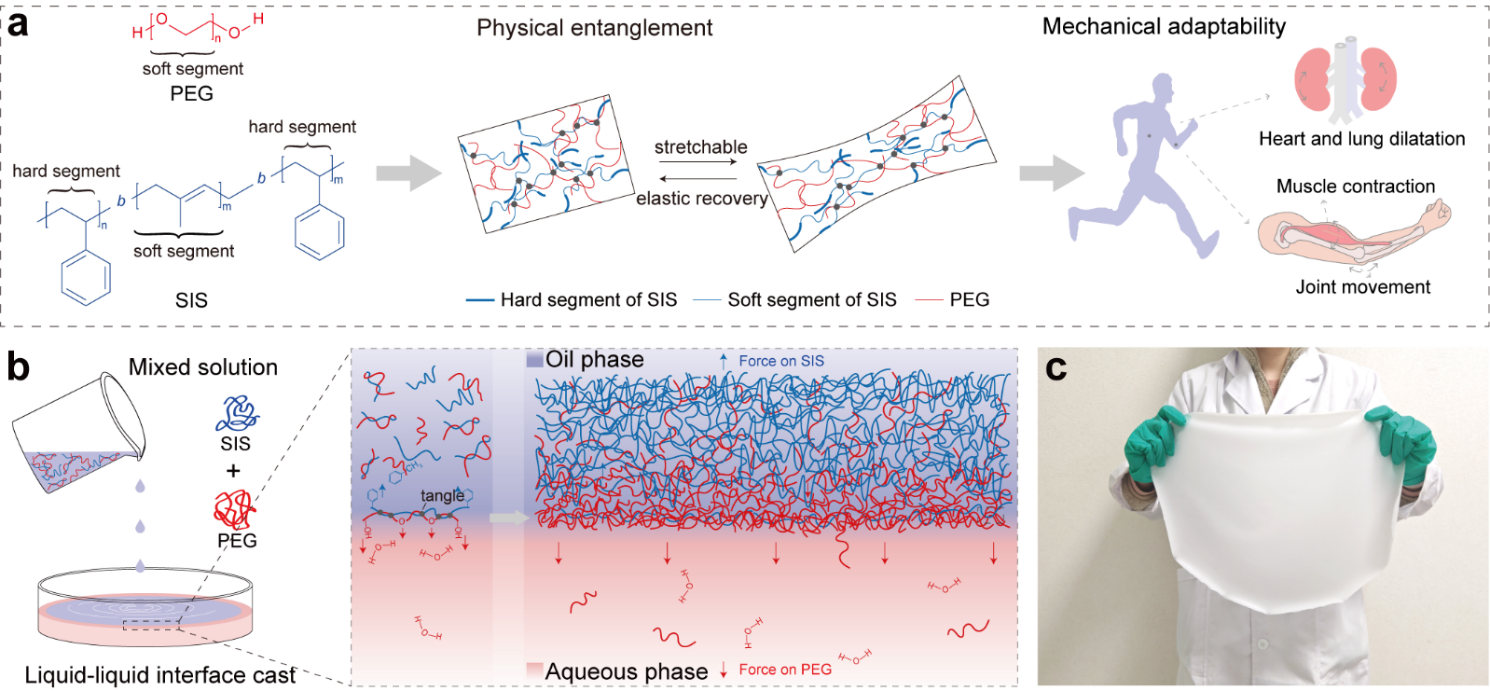
图1.PEG/SIS超柔性压电薄膜的构想与合成
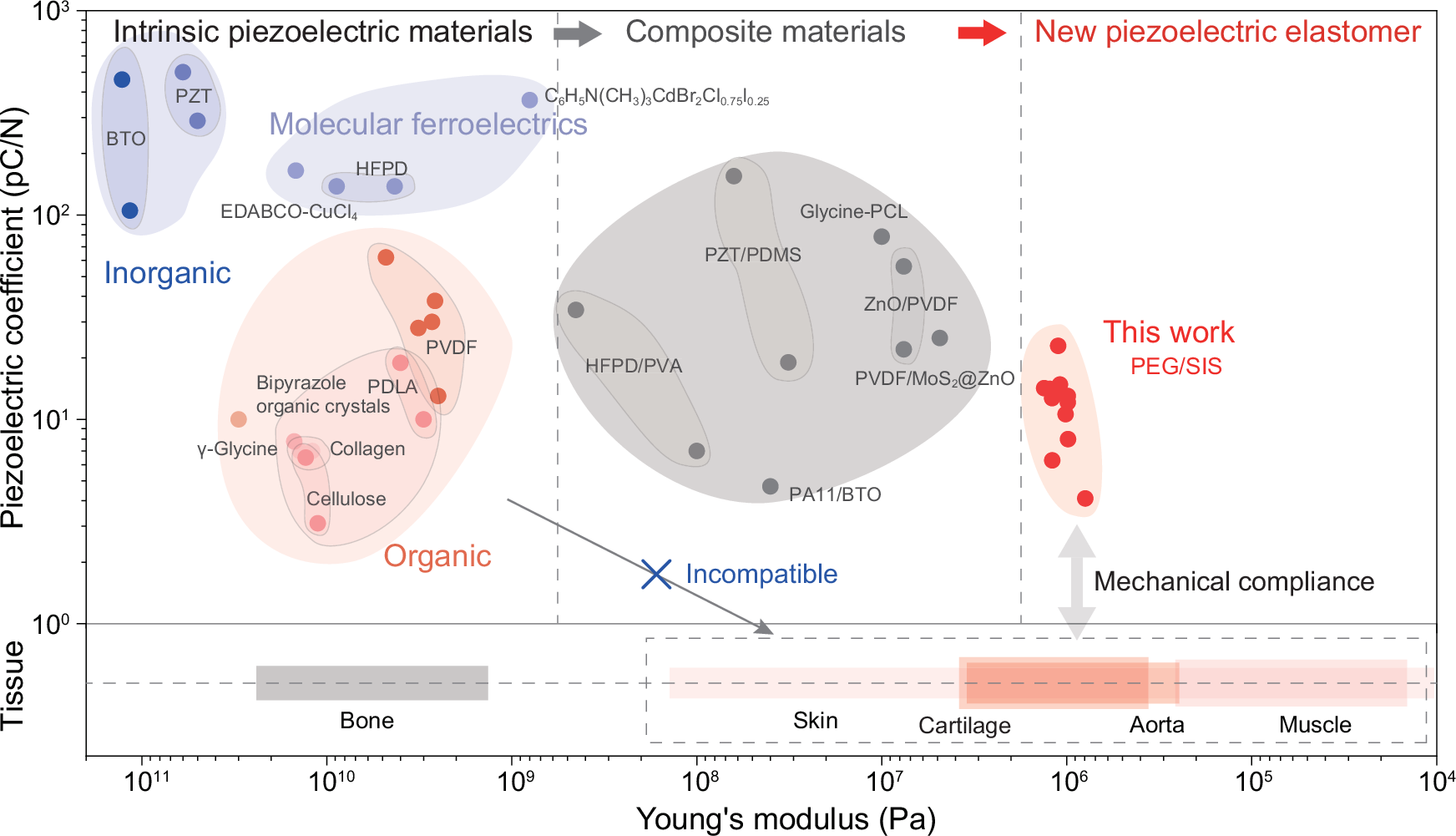
图2.PEG/SIS超柔性压电薄膜与传统压电材料在杨氏模量与压电性方面的对比
该技术为构建新型生物集成电子开辟新路径。“液-液界面极性工程从根本上解决了有机压电材料柔性和压电特性不可兼得的矛盾,”研究团队成员刘书海指出,“该策略有效破解了材料压电性与柔性的互斥难题。这种‘皮肤级’压电材料可无缝贴合人体器官,为植入式心脏监测、脑机接口及智能假肢提供材料支撑。”
研究工作由兰州大学材料与能源学院博士研究生张永康(第一作者)等人合作完成,刘书海青年教授和秦勇教授为本文通讯作者。研究得到国家自然科学基金、甘肃省自然科学基金和科技部国家重点研发计划项目支持。



 甘公网安备62010202000830号
甘公网安备62010202000830号